Принципы визуальной обработки изображений для фармацевтической инспекции
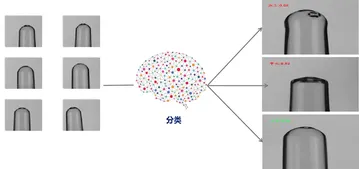
Визуальная обработка изображений с помощью машинного зрения позволяет обнаруживать дефекты или посторонние частицы в фармацевтических продуктах, таких как инъекционные растворы, лиофилизированные порошки и предварительно заполненные шприцы, путем анализа цифровых изображений, полученных с помощью камер или датчиков высокого разрешения. Процесс включает несколько ключевых этапов:
Классификация после обнаружения
После визуального контроля полученные характеристики сравниваются с заданными стандартами для выявления таких отклонений, как дефекты корпуса флакона, загрязнения или неравномерный уровень наполнения. На основании этого анализа несоответствующая продукция отбраковывается и автоматически регистрируется в системе.
Преимущества
- Неразрушающий метод тестирования: инспекция проводится бесконтактно, что позволяет сохранить целостность продукта.
- Высокая точность: метод визуального контроля более эффективен, чем ручная инспекция. Это позволяет выявлять дефекты микронного уровня (трещины, проколы, мелкие частицы, сколы, ворс и т.д.).
- Скорость и масштабируемость: возможность проверки тысячи единиц продукции в минуту делает систему идеальной для высокопроизводительных автоматизированных производственных линий.
- Стабильность процесса: снижение влияния человеческого фактора и обеспечение соответствия строгим нормативным стандартам (GMP).
- Гибкость проверки качества: алгоритмы можно настраивать для проверки широкого спектра лекарственных форм, включая таблетки, жидкости, а также различные типы упаковок.
Данный метод контроля качества повышает эффективность фармацевтического производства, сокращает количество отходов, а также гарантирует безопасность пациентов.
Визуальный контроль и соответствие нормативным требованиям
Визуальный контроль (ручной, автоматизированный) - является критически важным этапом фармацевтического производства. Этот метод обеспечивает стерильность и целостность фармацевтического продукта, помогая предотвратить загрязнение лекарственного средства видимыми частицами (волокна, частицы, сколы и т.д.).
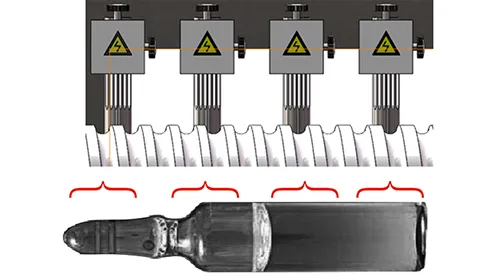
Автоматизированный визуальный контроль подразумевает использование промышленных камер высокого разрешения и передовых алгоритмов обработки изображений для быстрой и точной проверки лекарственных препаратов. Система подходит для крупномасштабного производства и обеспечивает высокий стандарт контроля, минимизируя влияние оператора.
Источники видимых посторонних частиц
Загрязнения, обнаруживаемые визуально, обычно делятся на внешние и внутренние
:
Внешние: не связанные с производственным процессом (волосы, волокна), не связанные с технологическим процессом (крахмальные гранулы, минеральная пыль). Посторонние частицы, попадающие в продукт, обычно носят случайный характер и могут создавать риск микробного загрязнения.
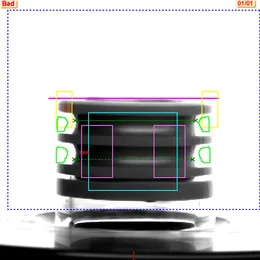
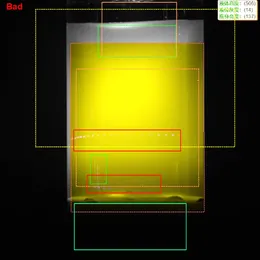
Примеры косметических дефектов и загрязнений видимыми частицами.
Нормативные требования и стандарты
Международные фармацевтические регламенты и стандарты качества устанавливают конкретные требования к визуальному контролю, чтобы гарантировать, что каждая партия инъекционных препаратов проходит строгий контроль качества. Хотя детали могут различаться в разных руководствах, существует множество общих требований к таким стандартам, как GMP (Надлежащая производственная практика), FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) и EMA (Европейское агентство по лекарственным средствам).
- 100% точность визуального контроля
Все инъекционные препараты должны проходить 100% визуальный контроль, что означает, что каждая упаковка и ее содержимое в каждой производственной партии должны быть проверены на отсутствие видимых частиц и дефектов. Это требование призвано минимизировать риск попадания посторонних частиц в лекарственные препараты.
- Стандарт по видимым частицам
Видимые частицы обычно определяются как частицы размером более 50 микрон в диаметре. Нормативные акты предусматривают, что инъекционные препараты должны быть свободны от видимых частиц. Фармакопея США (USP), Европейская фармакопея (EP) и Японская фармакопея (JP) предписывают этот стандарт. В процессе производства любая единица продукции, в которой обнаружены видимые частицы, должна быть отбракована.
Установленные стандарты помогают гарантировать качество продукции и обеспечивать безопасность пациентов, минимизируя риск воздействия вредных загрязняющих веществ.
Поскольку обнаружение видимых посторонних частиц является вероятностным событием, на него влияют такие факторы, как тип инъекционного препарата, рецептура продукта, свойства посторонних частиц, материал упаковки и инспектор. Поэтому, независимо от того, используется ли ручной или автоматизированный визуальный контроль, достичь 100% обнаружения видимых посторонних частиц сложно. Помимо исключения дефектной продукции посредством контроля, важно учитывать характеристики инъекционных препаратов, уделять особое внимание контролю процесса и оптимизировать методы контроля. Выявляя и отслеживая источники видимых посторонних частиц, можно предотвратить загрязнение в источнике и создать научную, систематическую систему контроля.